Bahamanian kali ini tentang termodinamika yah, selamat membaca.... :)
A. Usaha dan hukum I termodinamika Termodinamika
merupakan ilmu yang mempelajari hubungan kalor dan bentuk lain dari
energi. Kalor bergerak secara alami dari materi yang lebih panas ke
materi yang lebih dingin .Contohnya lemari es ,panas secara terus
menerus diambil dari ruangan dalam yang dingin dan dibuang ke udara luar
yang lebih panas ,itu sebabnya bagian samping dan belakang biasanya
hangat .
Dalam termodinamika dikenal dengan istilah sistem dan lingkungan .Sistem merupakan benda yang akan diteliti dan lingkungan merupakan semua benda yang ada dialam .
Energi dalam
Suatu gas yang berada dalam suhu tertentu dikatakan memiliki energi dalam. Energi dalam gas berkaitan dengan suhu gas tersebut dan merupakan sifat mikroskopik gas tersebut. Meskipun gas tidak melakukan atau menerima usaha, gas tersebut dapat memiliki energi yang tidak tampak tetapi terkandung dalam gas tersebut yang hanya dapat ditinjau secara mikroskopik.
untuk gas diatomik

Dimana perubahan energi dalam adalah perubahan energi dalam gas, n adalah jumlah mol gas, R adalah konstanta umum gas (R = 8,31 J mol−1 K−1, dan perubahan suhu adalah perubahan suhu gas (dalam kelvin).
Hukum I Termodinamika
Proses Isobarik
 Sebelumnya telah dituliskan bahwa perubahan energi dalam sama dengan kalor yang diserap gas pada volume konstan
Sebelumnya telah dituliskan bahwa perubahan energi dalam sama dengan kalor yang diserap gas pada volume konstan
Proses Adiabatik
B. Siklus termodinamika dan hukum II termodinamika
1. Siklus Carnot
Berdasarkan sifatnya siklus dibagi menjadi 2 ,yaitu siklus reversible (dapat balik) dan siklus irreversible (tidak dapat balik). Siklus carnot termasuk siklus reversible.
- pada proses A-B terjadi ekspansi isotermik
- pada proses B-C terjadi ekspansi adiabatik
- pada proses C-D terjadi pemampatan isotermik
- pada proses D-A terjadi pemampatan adiabatik
Mesin kalor dan mesin pendingin menggunakan siklus energi kalor secara spontan dan tidak spontan. Jika mesin kalor kalor menyerap energi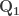 dari benda bersuhu tinggi ~ sebab
dari benda bersuhu tinggi ~ sebab 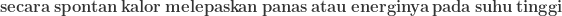 dan benda yang bersuhu rendah akan secara spontan menyerap energi
tersebut. Benda bersuhu rendah dinyatakan mempunyai energi sebesar
dan benda yang bersuhu rendah akan secara spontan menyerap energi
tersebut. Benda bersuhu rendah dinyatakan mempunyai energi sebesar 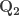 .
.
Berdasar prinsip mesin pemanas tersebut, maka
perhitungan efisiensi mesin panas menjadi :
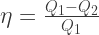 x 100%
x 100%
Efisiensi mesin pendingin Carnot adalah sebagai berikut :
K=Q2/Q1-Q2

karena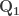 selalu lebih besar nilainya dari
selalu lebih besar nilainya dari 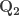 maka hasil pembagian fungsi tersebut selalu lebih dari angka 1.
maka hasil pembagian fungsi tersebut selalu lebih dari angka 1.

2. Siklus Otto
Siklus mesin bakar atau biasa disebut siklus Otto ..
- pada proses 1-2 terjadi pemampatan adiabatik
- pada proses 2-3 terjadi isokhorik
- pada proses 3-4 terjadi ekspansi adiabatik
- pada proses 4-1 terjadi iskhorik
Usaha yang dilakukan sistem pada siklus Otto adalah :
W= Q1 - Q2
Efisiensi siklus Otto adalah :
efisiensi= 1 - Q2/Q1
3. Siklus Diesel

- pada proses 1-3 terjadi pemampatan adiabatik
- pada proses 3-3a langkah daya pertama ekspansi isobarik
- pada proses 3a-4 terjadi ekspansi adiabatik
- pada proses 4-1 terjadi penurunan suhu
4. Siklus Rankine
Siklus mesin uap disebut juga siklus Rankine.
Dalam termodinamika dikenal dengan istilah sistem dan lingkungan .Sistem merupakan benda yang akan diteliti dan lingkungan merupakan semua benda yang ada dialam .
Energi dalam
Suatu gas yang berada dalam suhu tertentu dikatakan memiliki energi dalam. Energi dalam gas berkaitan dengan suhu gas tersebut dan merupakan sifat mikroskopik gas tersebut. Meskipun gas tidak melakukan atau menerima usaha, gas tersebut dapat memiliki energi yang tidak tampak tetapi terkandung dalam gas tersebut yang hanya dapat ditinjau secara mikroskopik.
Berdasarkan teori kinetik gas, gas
terdiri atas partikel-partikel yang berada dalam keadaan gerak yang
acak. Gerakan partikel ini disebabkan energi kinetik rata-rata dari
seluruh partikel yang bergerak. Energi kinetik ini berkaitan dengan suhu
mutlak gas. Jadi, energi dalam dapat ditinjau sebagai jumlah
keseluruhan energi kinetik dan potensial yang terkandung dan dimiliki
oleh partikel-partikel di dalam gas tersebut dalam skala mikroskopik.
Dan, energi dalam gas sebanding dengan suhu mutlak gas. Oleh karena itu,
perubahan suhu gas akan menyebabkan perubahan energi dalam gas. Secara
matematis, perubahan energi dalam gas dinyatakan sebagai
untuk gas monoatomik

untuk gas diatomik

Dimana perubahan energi dalam adalah perubahan energi dalam gas, n adalah jumlah mol gas, R adalah konstanta umum gas (R = 8,31 J mol−1 K−1, dan perubahan suhu adalah perubahan suhu gas (dalam kelvin).
Hukum I Termodinamika
Jika
kalor diberikan kepada sistem, volume dan suhu sistem akan bertambah
(sistem akan terlihat mengembang dan bertambah panas). Sebaliknya, jika
kalor diambil dari sistem, volume dan suhu sistem akan berkurang (sistem
tampak mengerut dan terasa lebih dingin). Prinsip ini merupakan hukum
alam yang penting dan salah satu bentuk dari hukum kekekalan energi.
Sistem
yang mengalami perubahan volume akan melakukan usaha dan sistem yang
mengalami perubahan suhu akan mengalami perubahan energi dalam. Jadi,
kalor yang diberikan kepada sistem akan menyebabkan sistem melakukan
usaha dan mengalami perubahan energi dalam. Prinsip ini dikenal sebagai
hukum kekekalan energi dalam termodinamika atau disebut hukum I
termodinamika. Secara matematis, hukum I termodinamika dituliskan
sebagai
perubahan kalor (Q)=perubahan usaha(W)+ perubahan energi dalam(U)
Dimana Q adalah kalor, W adalah usaha, dan adalah perubahan energi dalam. Secara sederhana, hukum I termodinamika dapat dinyatakan sebagai berikut.
Jika suatu benda (misalnya krupuk)
dipanaskan (atau digoreng) yang berarti diberi kalor Q, benda (krupuk)
akan mengembang atau bertambah volumenya yang berarti melakukan usaha W
dan benda (krupuk) akan bertambah panas (coba aja dipegang, pasti panas deh!) yang berarti mengalami perubahan energi dalam .
Proses Isotermik
Suatu
sistem dapat mengalami proses termodinamika dimana terjadi
perubahan-perubahan di dalam sistem tersebut. Jika proses yang terjadi
berlangsung dalam suhu konstan, proses ini dinamakan proses isotermik.
Karena berlangsung dalam suhu konstan, tidak terjadi perubahan energi
dalam ( perubahan energi dalam = 0) dan berdasarkan hukum I termodinamika kalor yang diberikan sama dengan usaha yang dilakukan sistem (Q = W).
Proses isotermik dapat digambarkan dalam grafik p – V di bawah ini. Usaha yang dilakukan sistem dan kalor dapat dinyatakan sebagai
Proses Isokhorik
Jika
gas melakukan proses termodinamika dalam volume yang konstan, gas
dikatakan melakukan proses isokhorik. Karena gas berada dalam volume
konstan (perubahan kalor= perubahan energi dalam ), gas tidak melakukan
usaha (W = 0) dan kalor yang diberikan sama dengan perubahan energi dalamnya. Kalor di sini dapat dinyatakan sebagai kalor
gas pada volume konstan QV.
QV = perubahan energi dalamProses Isobarik
Jika
gas melakukan proses termodinamika dengan menjaga tekanan tetap
konstan, gas dikatakan melakukan proses isobarik. Karena gas berada
dalam tekanan konstan, gas melakukan usaha (W = p.perubahan volume). Kalor di sini dapat dinyatakan sebagai kalor gas pada tekanan konstan Qp. Berdasarkan hukum I termodinamika, pada proses isobarik berlaku
QV =perubahan energi dalam
Dari sini usaha gas dapat dinyatakan sebagai
W = Qp − QV
Jadi, usaha yang dilakukan oleh gas (W) dapat dinyatakan sebagai selisih energi (kalor) yang diserap gas pada tekanan konstan (Qp) dengan energi (kalor) yang diserap gas pada volume konstan (QV).
Proses Adiabatik
Dalam proses adiabatik tidak ada kalor yang masuk (diserap) ataupun keluar (dilepaskan) oleh sistem (Q = 0). Dengan demikian, usaha yang dilakukan gas sama dengan perubahan energi dalamnya (-perubahan usaha = perubahan energi dalam)
Jika suatu sistem berisi gas yang mula-mula mempunyai tekanan dan volume masing-masing p1 dan V1 mengalami proses adiabatik sehingga tekanan dan volume gas berubah menjadi p2 dan V2, usaha yang dilakukan gas dapat dinyatakan sebagai
B. Siklus termodinamika dan hukum II termodinamika
1. Siklus Carnot
Berdasarkan sifatnya siklus dibagi menjadi 2 ,yaitu siklus reversible (dapat balik) dan siklus irreversible (tidak dapat balik). Siklus carnot termasuk siklus reversible.
- pada proses A-B terjadi ekspansi isotermik
- pada proses B-C terjadi ekspansi adiabatik
- pada proses C-D terjadi pemampatan isotermik
- pada proses D-A terjadi pemampatan adiabatik
Mesin kalor dan mesin pendingin menggunakan siklus energi kalor secara spontan dan tidak spontan. Jika mesin kalor kalor menyerap energi
Berdasar prinsip mesin pemanas tersebut, maka
perhitungan efisiensi mesin panas menjadi :
Efisiensi mesin pendingin Carnot adalah sebagai berikut :
K=Q2/Q1-Q2

karena

2. Siklus Otto
Siklus mesin bakar atau biasa disebut siklus Otto ..
- pada proses 1-2 terjadi pemampatan adiabatik
- pada proses 2-3 terjadi isokhorik
- pada proses 3-4 terjadi ekspansi adiabatik
- pada proses 4-1 terjadi iskhorik
Usaha yang dilakukan sistem pada siklus Otto adalah :
W= Q1 - Q2
Efisiensi siklus Otto adalah :
efisiensi= 1 - Q2/Q1
3. Siklus Diesel

- pada proses 1-3 terjadi pemampatan adiabatik
- pada proses 3-3a langkah daya pertama ekspansi isobarik
- pada proses 3a-4 terjadi ekspansi adiabatik
- pada proses 4-1 terjadi penurunan suhu
4. Siklus Rankine
Siklus mesin uap disebut juga siklus Rankine.








0 Tanggapan :
Post a Comment